2018年11月13日,国际知名期刊Angewandte Chemie International Edition (IF 12.102,JCR1区)在线发表了中心博士后楚成超为第一作者的研究论文《Zinc(II)-dipicolylamine Coordination Nanotheranostics: Toward Synergistic Nanomedicine by Combined Photo/gene Therapy》。
近年来,通过金属离子和药物分子直接组装制备成金属有机纳米结构用于疾病的诊断和治疗逐步引起科研人员的重视。相对比与传统的亲疏水性药物自组装,这种金属有机纳米结构不仅能够提高药物装载和递送能力,而且能够增加药物在生理环境中的循环稳定性。课题组前期研究了临床抗肿瘤光敏剂华卟啉钠(DVDMS),FDA批准药物吲哚菁绿ICG与多种金属离子的配位组装机制并发表了一系列的成果,如纳米药物的体内自组装体系(Adv. Mater., 2017, 29:1605928);肿瘤微环境响应的超小纳米自组装体系(J. Am. Chem. Soc. 2018, 140, 14980-14989),以及微泡内部原位形成Fe3+/ICG自组装纳米材料用于肝癌声动力治疗等(Nanoscale Horiz., 2018, DOI:10.1039/C8NH00276B;申请专利号:201810461899.5)。
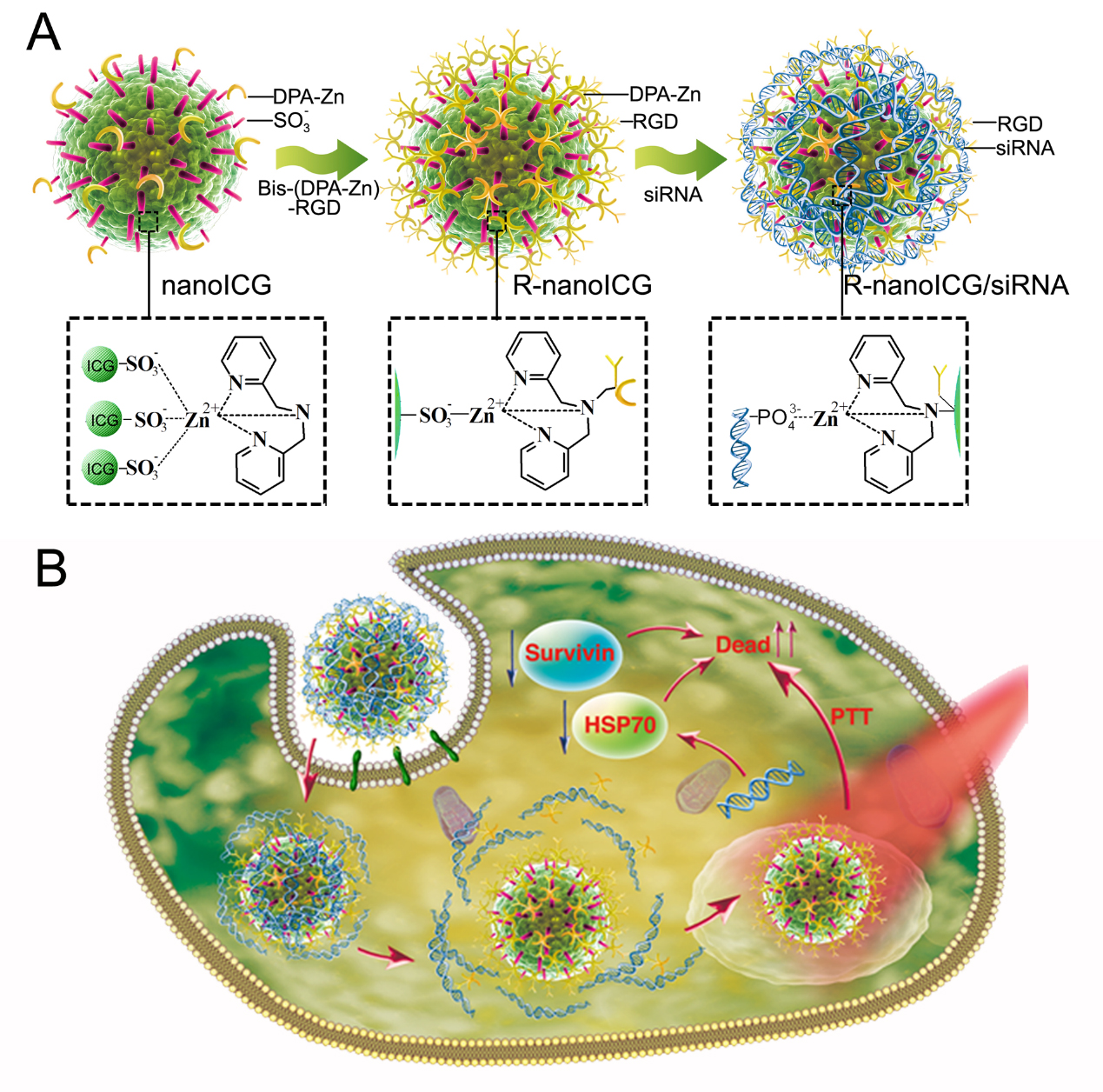
在本研究中,楚成超等发现Zn(II)-二甲基吡啶胺(DPA-Zn)具有比Zn2+更强的磺酸根结合能力,并且依靠独特的分子空间结构与ICG分子结合能够形成结构稳定、形貌均一的ICG纳米结构(nanoICG)。基于DPA-Zn的引入,nanoICG具有优于小分子ICG的光热、荧光和光声性能。进一步在nanoICG表面修饰RGD多肽(R-nanoICG)之后可以增加survivin-siRNA(S-siRNA)在体内的递送并实现肿瘤的基因和光热协同治疗效果。这种新型的金属有机纳米结构作为药物递送载体具有以下的优势:(1)制备方法简单,具有较好的生物活性;(2)多种不同功能的集成进行靶向性治疗;(3)修饰方法简单并能够根据联合治疗的目的设计多种功能基团;(4)较好的生物相容性和临床转换性,拓展纳米制剂的制备策略和联合治疗方案。
楚成超于2014年加入中心刘刚老师小组,2018年6月获得博士学位并继续留在中心开展博士后工作,致力于多功能分子探针研发,迄今已在Angew Chem(IF 12.102)、Adv Mater(IF 21.95)、Adv Sci(IF 12.441)等知名学术期刊发表第一作者SCI论文11篇。上述系列论文通讯作者为刘刚教授并得到了科技部重大专项课题、973课题、国家自然科学基金优秀青年科学基金等项目的支持。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.201812482